上海一研生物科技有限公司
10 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
- 查看全部分类
- 实验抗体
- 酶联免疫elisa分析试剂盒
- RNA/DNA提取
- 生化试剂
- 标准品
- ATCC细胞
- 抗体
- 菌种
- elisa检测试剂盒
- 生物抗体
- USP标准品
- 科研抗体
- 原代细胞
- 科研抗体
- 生化试剂类
- PCR检测试剂盒
- 培养基
- 生化检测试剂盒
- 进口品牌
- 代理进口品牌
- 生物碱
- 黄酮
- 查尔酮
- 氧杂蒽酮
- 木脂素
- 香豆素
- 苯丙素
- 其它酚类
- 三萜
- 药物杂质及中间体
- 其它天然产物
- 蒽醌
- 其它醌类
- 甾体
- 二萜
- 其它萜类
- 环烯醚萜
- 倍半萜
- 中药对照品
- 质粒
- 定做种属检测试剂盒/中药材鉴定试剂盒
- 细胞生物学试剂
- DRG试剂盒
- 荧光定量PCR试剂盒
- 对照品
- 菌种库
- 细胞株
- 耗材和仪器
- 分子生物学试剂盒
- 培养基
- ELISA Kit
- ELISA检测试剂盒
- 细胞培养
- 标准溶液
- LAMP试剂盒
- 基因PCR试剂盒
- 鉴定PCR试剂盒
- 进口抗体
- 抑制剂
推荐产品
公司新闻/正文
细胞分离液的配置与使用方法
880 人阅读发布时间:2024-10-22 16:51
不同浓度(密度)分离液的制备: 先用9份分离液与1份8.5% NaCl或1.5MPBS混合达到生理性渗透压,然后用生理溶液(0.85% NaCl或0.15M PBS)稀释到所需浓度。
不连续密度梯度层的制备: 先将试管壁用牛血清湿润,除去多余血清,这种预处理可使逐层叠加的液平稳沿管壁流下,使形成满意的界面。在制备过程中一般用长针头注射器从高密度向低密度逐层放置,有时相邻两层比重相差不大时,可将液放入注射器中,小针头斜面紧贴管壁,任其自然慢慢流下。
装样:样品体积和细胞浓度根据不同细胞而异,一般加样体积不宜过大,细胞浓度也不可过高,否则会影响细胞的分离和回收。
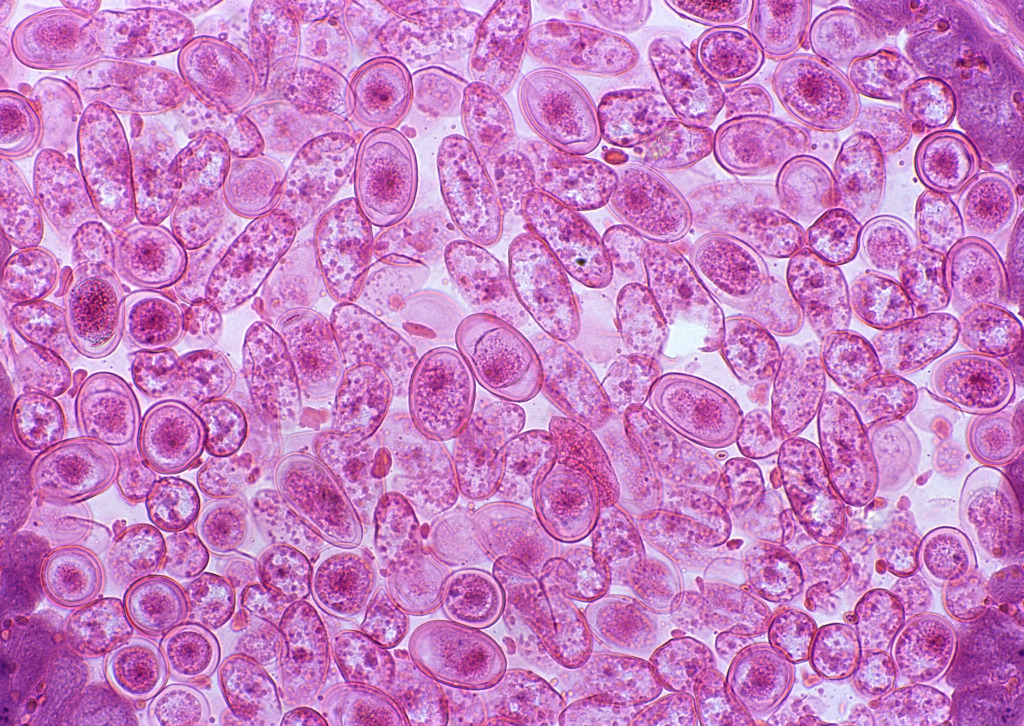
离心:一般采用离心力为400g,时间20~25min。由于多层之间密度差别不大,因此离心机加速、降速时要慢,要平稳。完成离心步骤后,接下来的操作至关重要,即样品的分层与收集。轻轻取出离心管,此时应能观察到明显的分层现象,不同密度的细胞或组分被清晰地分隔开来。为了避免破坏这精细的分层结构,使用长柄吸管或移液器沿管壁缓缓吸取目标层,确保不混入相邻层的杂质。
对于某些需要更高纯度样品的实验,可能还需进行二次离心或梯度离心,以进一步纯化目标细胞或组分。在二次处理过程中,需根据首次离心结果调整离心参数,如离心力、时间或离心管中溶液的密度梯度,以达到最佳分离效果。
完成收集后,应立即对目标样品进行必要的处理或保存。若需进行后续培养或实验分析,应确保使用无菌技术操作,并尽快将样品转移至适当的培养液或缓冲液中,以保持细胞的活性和稳定性。同时,记录好每一步操作的时间、条件及观察结果,这对实验结果的解析和复现至关重要。
此外,实验过程中产生的废弃物应按照实验室规定进行分类处理,确保生物安全和环境保护。最后,回顾整个实验流程,总结经验教训,不断优化实验方案,为未来的科学研究打下更加坚实的基础。
取样:当所要分离的细胞绝大部分在两层的界面时,可逐层去除液后收集界面部位的细胞;有时大部分细胞位于层中,则需要逐层收集。收获含有液的细胞经2次洗涤后可供培养或检测用。